Rétinopathie diabétique : stades, fond d'œil et traitements anti-VEGF
Rétinopathie diabétique : la complication oculaire n°1 du diabète, première cause de cécité acquise avant 65 ans en France. Stades R0-R3 + œdème maculaire, dépistage annuel, contrôle glycémique strict, photocoagulation laser, injections intravitréennes d'anti-VEGF (Lucentis®, Eylea®, Vabysmo®) et corticostéroïdes. Sources HAS, ANSM, SFO.
Tout diabétique craint la cécité — et c'est légitime. La rétinopathie diabétique est la complication oculaire n°1 du diabète et reste, en France comme dans la majorité des pays développés, la première cause de cécité acquise chez l'adulte avant 65 ans. Le pilier Diabète de type 21 couvre la maladie globale ; le cluster Complications du diabète2 les expose. Cet article traite spécifiquement de la rétinopathie — physiopathologie, stades, dépistage, traitements actuels. Bonne nouvelle : la prise en charge a été transformée en 20 ans par les injections intravitréennes d'anti-VEGF, qui ont fait reculer la cécité.
Comment le diabète atteint la rétine — la microangiopathie
L'hyperglycémie chronique endommage l'endothélium vasculaire de tout le corps — c'est la microangiopathie diabétique. Au niveau rétinien, les modifications successives sont :
- Épaississement de la membrane basale capillaire et perte de péricytes (cellules de soutien des capillaires rétiniens).
- Fragilisation des capillaires avec apparition de microanévrysmes (premiers signes visibles au fond d'œil) et de microhémorragies.
- Rupture de la barrière hémato-rétinienne → fuite plasmatique → œdème rétinien et exsudats secs (dépôts lipidiques jaunes).
- Occlusion capillaire progressive → ischémie rétinienne → libération de VEGF (Vascular Endothelial Growth Factor).
- Néovascularisation pathologique en réponse à l'ischémie — c'est le passage à la rétinopathie proliférante, à haut risque d'hémorragie et de décollement de rétine.
- Œdème maculaire diabétique (OMD) — accumulation de liquide au niveau de la macula, zone centrale de la vision, possible à tout stade et principale cause de baisse de vision.
Les stades évolutifs — classification ALFEDIAM / HAS
La classification française ALFEDIAM (Association de Langue Française pour l'Étude du Diabète et des Maladies métaboliques), retenue par la HAS, distingue quatre stades de rétinopathie selon les anomalies vasculaires visibles au fond d'œil, indépendamment de l'œdème maculaire (qui se cote à part). La galerie ci-dessous illustre les principaux stades sur des vues d'artiste de fond d'œil.
Vues d'artiste illustrant la progression des anomalies vasculaires visibles au fond d'œil selon la classification ALFEDIAM / HAS. Tout diabétique doit bénéficier d'un fond d'œil annuel — la majorité des stades précoces sont asymptomatiques.
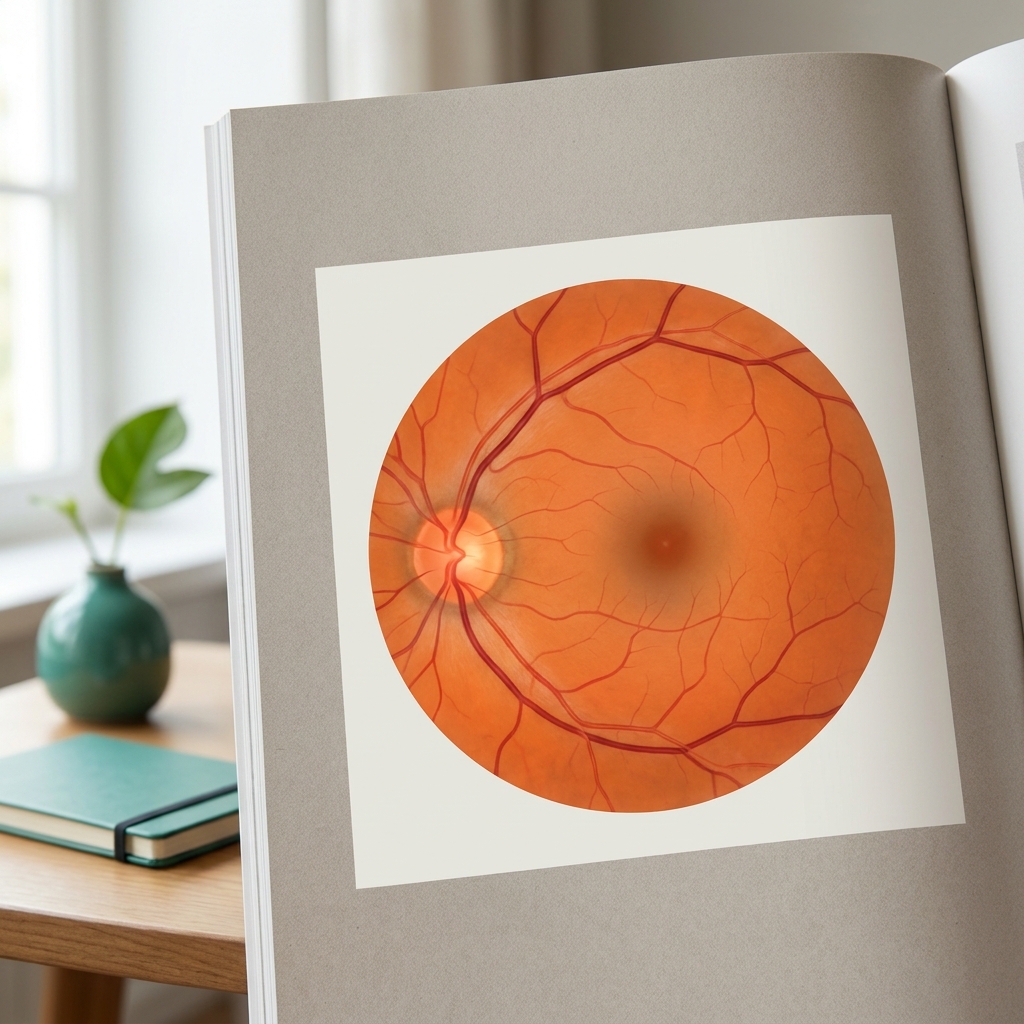
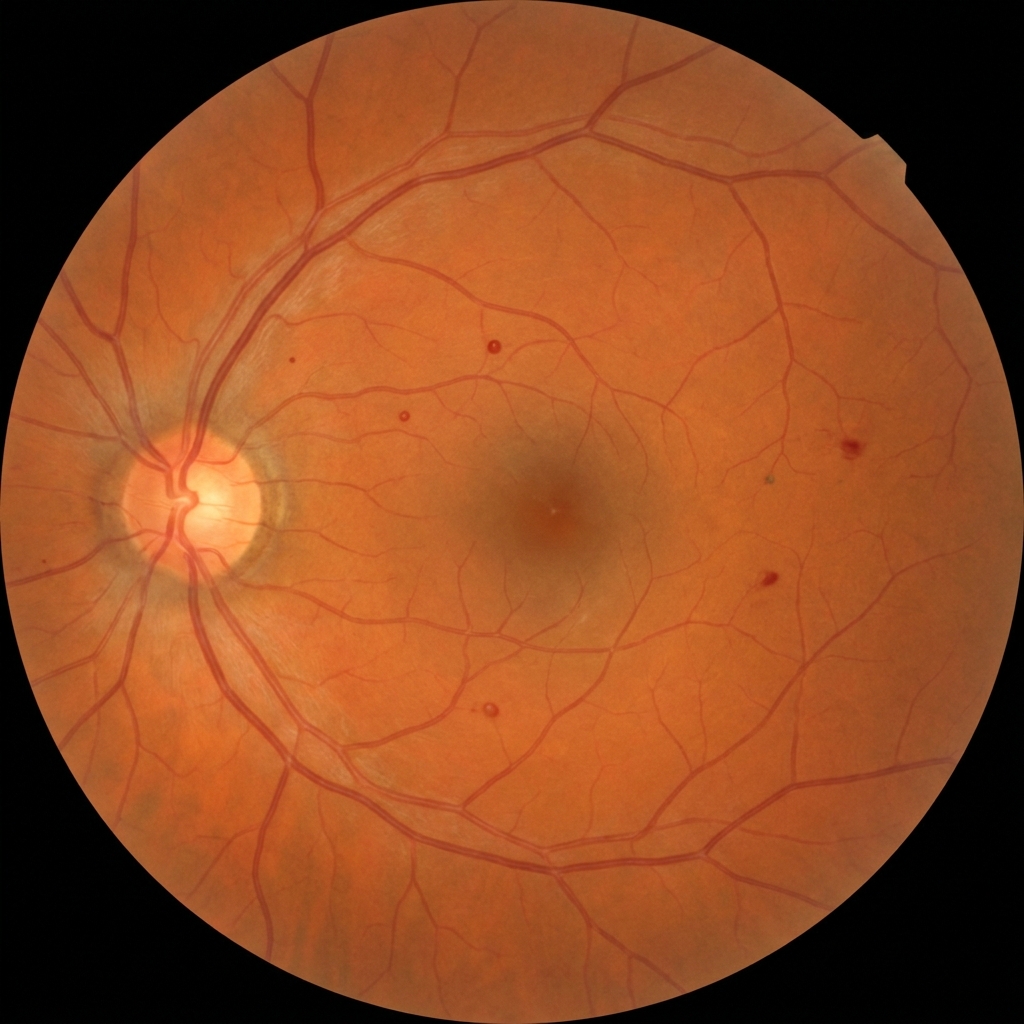
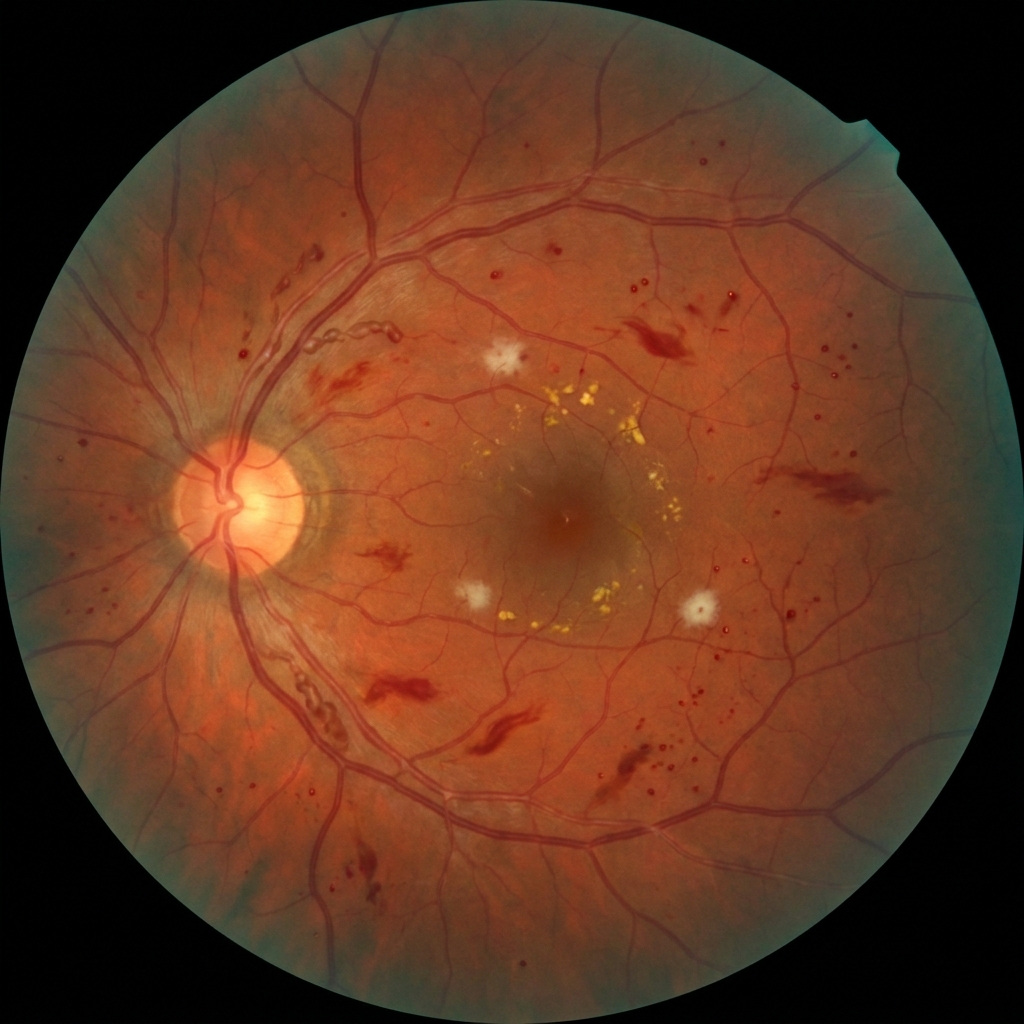
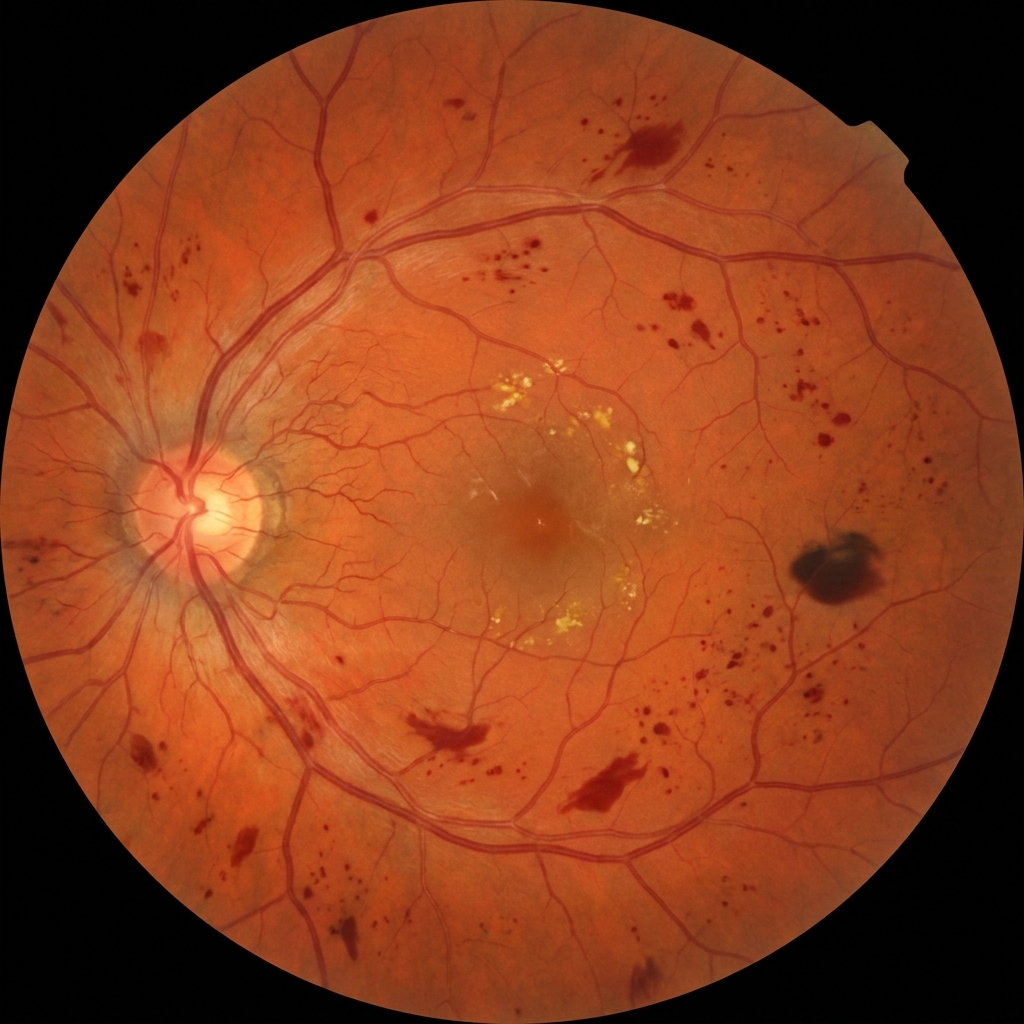
Vues d'artiste éducatives générées par IA, conçues pour illustrer schématiquement les principaux stades de la rétinopathie diabétique selon la classification ALFEDIAM / HAS. Le fond d'œil réel d'un patient peut présenter des associations de lésions et requiert une lecture par ophtalmologiste qualifié.
Le dépistage — le pilier de la prévention de la cécité
La rétinopathie diabétique est asymptomatique tant qu'elle n'a pas atteint le stade proliférant ou maculaire — d'où l'importance d'un dépistage systématique annuel chez tout patient diabétique. Les modalités selon la HAS :
- Diabète de type 1 — premier fond d'œil à partir de 5 ans d'évolution (ou à l'adolescence si début pédiatrique), puis annuel.
- Diabète de type 2 — fond d'œil dès le diagnostic (jusqu'à 30 % ont déjà une rétinopathie au moment du diagnostic — diabète méconnu prolongé), puis annuel.
- Grossesse diabétique — fond d'œil au 1ᵉʳ trimestre, puis trimestriel pendant toute la grossesse — la grossesse peut aggraver rapidement une rétinopathie préexistante.
- Téléophtalmologie — depuis 2022, l'orthoptiste peut réaliser des rétinophotographies non mydriatiques en cabinet ou en centre de santé, télétransmises à l'ophtalmologiste pour lecture différée. Couvre les zones désertifiées et accélère l'accès. Validé HAS et remboursé par l'Assurance Maladie.
- OCT maculaire en complément si suspicion d'œdème maculaire ou si rétinopathie évolutive.
En cas de baisse visuelle, de vision floue centrale, de scotomes (taches noires), de myodésopsies (corps flottants) abondantes nouvelles ou de vision déformée (métamorphopsies) chez un diabétique, consultation ophtalmologique en urgence (dans la semaine) — il peut s'agir d'une hémorragie intravitréenne, d'un décollement de rétine ou d'un œdème maculaire.
Premier pilier — le contrôle glycémique, tensionnel et lipidique
Avant tout traitement spécifique, la maîtrise des facteurs métaboliques est le pilier fondamental — c'est ce qui prévient l'apparition et ralentit la progression de la rétinopathie. Les preuves les plus solides viennent de l'étude UKPDS (United Kingdom Prospective Diabetes Study) et de l'étude DCCT (Diabetes Control and Complications Trial) :
- Chaque baisse de 1 % d'HbA1c réduit le risque de complications microvasculaires (incluant la rétinopathie) de 21 % en moyenne.
- Cible : HbA1c < 7 % chez l'adulte diabétique sans comorbidités, individualisée selon l'âge, l'espérance de vie et le risque d'hypoglycémie.
- Cible tensionnelle : < 140/85 mmHg (voire < 130/80 mmHg chez le sujet jeune et tolérant). Voir cluster HTA essentielle3.
- Cible lipidique : LDL-cholestérol < 0,7 g/L chez le diabétique à très haut risque vasculaire (statine systématique).
- Arrêt du tabac — facteur majeur d'aggravation de la microangiopathie.
- Contrôle du surpoids, activité physique régulière, alimentation équilibrée — voir cluster alimentation diabète4.
Deuxième pilier — la photocoagulation laser pan-rétinienne
La photocoagulation pan-rétinienne (PPR) au laser argon ou laser frequency-doubled YAG reste la technique de référence dans la rétinopathie proliférante depuis les essais DRS et ETDRS des années 1970-80. Elle consiste à appliquer 1500 à 3000 impacts laser répartis sur la rétine périphérique (la macula est épargnée) en 2 à 4 séances ambulatoires.
Mécanisme : destruction contrôlée des zones d'ischémie périphérique → réduction de la production de VEGF → régression des néovaisseaux → prévention des complications (hémorragie intravitréenne, décollement, glaucome néovasculaire).
Effets indésirables : léger rétrécissement du champ visuel périphérique, baisse de la vision nocturne et de l'adaptation à l'obscurité, sensibilité aux contrastes diminuée. Effets permanents, mais qui restent compatibles avec une vie quasi normale (sauf conduite nocturne intensive).
La PPR est indispensable en RP, parfois combinée à des injections d'anti-VEGF pour accélérer la régression des néovaisseaux et améliorer la vision si OMD associé. Le laser focal (sur des microanévrysmes spécifiques) reste une option pour certains œdèmes maculaires avec point de fuite identifié, bien que largement supplanté par les anti-VEGF.
Troisième pilier — les injections intravitréennes d'anti-VEGF
L'introduction des anti-VEGF en injection intravitréenne à partir des années 2000 a révolutionné la prise en charge de l'œdème maculaire diabétique et de la rétinopathie proliférante. Le VEGF (Vascular Endothelial Growth Factor) est la principale cytokine responsable de la néovascularisation pathologique et de la perméabilité capillaire excessive ; son inhibition bloque ces deux mécanismes.
| Molécule (nom commercial) | Cible | Posologie initiale OMD | Maintenance | Particularités |
|---|---|---|---|---|
| Ranibizumab (Lucentis®) | VEGF-A | 1 injection / mois × 3 puis adaptation | Mensuelle puis espacement progressif PRN ou Treat-and-Extend | AMM 2011 OMD ; biosimilaires depuis 2022 (Byooviz®, Ximluci®) |
| Aflibercept (Eylea®) | VEGF-A, VEGF-B, PlGF | 1 injection / mois × 5 puis bimestrielle | Bimestrielle, Treat-and-Extend possible jusqu'à 16 sem | AMM 2014 OMD ; haute dose 8 mg (Eylea HD®) disponible depuis 2024 pour espacer encore |
| Faricimab (Vabysmo®) | VEGF-A + Angiopoïétine-2 | 1 injection / mois × 4-6 puis Treat-and-Extend | Espacement possible jusqu'à 16 sem | AMM 2022 OMD ; double mécanisme (anti-VEGF + anti-Ang2) — meilleure durabilité |
| Brolucizumab (Beovu®) | VEGF-A (mini-anticorps) | 1 injection / mois × 6 puis trimestrielle | Trimestrielle possible | AMM OMD 2022 ; rare effet indésirable d'inflammation intraoculaire |
| Bévacizumab (Avastin®) | VEGF-A | Off-label en ophtalmologie | Mensuelle initiale | Hors AMM ophtalmologique en France, accessible dans certains contextes hospitaliers |
Les injections sont réalisées en cabinet d'ophtalmologie sous anesthésie locale (collyre), strict aseptique. La douleur est minime. Effets indésirables principaux : inconfort transitoire, flou visuel de quelques heures, corps flottants transitoires. Complications rares mais sérieuses : endophtalmie infectieuse (1/2000 à 1/5000 injections), déchirure rétinienne, augmentation de la pression intraoculaire.
Le Pr Ramin Tadayoni (Hôpital Lariboisière AP-HP) explique le mécanisme du traitement anti-VEGF de l'œdème maculaire diabétique et le bénéfice du faricimab bispécifique (VEGF + Ang2) pour espacer les injections.
- Le mécanisme principal du traitement de l'œdème maculaire diabétique repose sur la neutralisation du VEGF, qui rend les vaisseaux sanguins anormaux moins perméables.
- Le faricimab (Vabysmo®) est le premier anticorps bispécifique qui neutralise simultanément le VEGF et l'angiopoïétine-2.
- Le ciblage de l'angiopoïétine-2 retarde la récidive de l'œdème, permettant d'espacer les injections jusqu'à 3 mois.
- L'imagerie OCT (Tomographie par Cohérence Optique) montre une résorption rapide et complète du liquide intra-rétinien après traitement.
- Le bénéfice clinique est observable sur l'amélioration de l'acuité visuelle des patients traités.
Corticostéroïdes intravitréens et vitrectomie
Quand les anti-VEGF sont insuffisants ou contre-indiqués, deux options secondaires :
- Implant intravitréen de dexaméthasone (Ozurdex®, AMM 2010 dans l'OMD) — relargage prolongé sur 3-6 mois. Réservé aux patients pseudophakes (avec cristallin artificiel) — risque accru de cataracte chez le phake. Surveillance de la pression intraoculaire obligatoire (hypertonie iatrogène).
- Implant de fluocinolone (Iluvien®) — relargage prolongé sur 3 ans. Réservé aux OMD chroniques résistants aux anti-VEGF.
- Vitrectomie chirurgicale — indispensable en cas d'hémorragie intravitréenne non résolutive, de décollement de rétine tractionnel, ou de membrane épi-rétinienne compliquant l'OMD. Réalisée sous anesthésie locale par 3 micro-ports de 25 ou 27 gauges, en chirurgie ambulatoire.
Ce que l'avenir apporte — recherche actuelle
Plusieurs pistes prometteuses en cours d'évaluation :
- Anti-VEGF à durée d'action prolongée — l'aflibercept haute dose 8 mg (Eylea HD®, AMM 2024) permet d'espacer les injections jusqu'à 16 semaines.
- Thérapie génique — injection intravitréenne ou sous-rétinienne d'un vecteur viral codant pour un anti-VEGF endogène, possible « one-shot » durable. Études RGX-314, 4D-150 en phase 2-3.
- Anti-Ang2 + anti-VEGF — le faricimab est la première molécule de cette classe ; d'autres en développement.
- Petites molécules orales ciblant l'inflammation rétinienne (essais en cours).
- Intelligence artificielle pour le dépistage automatisé du fond d'œil — déjà déployée dans plusieurs régions, validation HAS en cours.
La rétinopathie diabétique ne signifie plus la cécité inéluctable qu'elle représentait il y a 30 ans. Le couple contrôle métabolique strict + dépistage annuel + traitement précoce permet aujourd'hui à la majorité des patients diabétiques de conserver une vision fonctionnelle tout au long de leur vie.
Questions fréquentes
Mon diabète est-il « grave » pour mes yeux ?
Le risque de rétinopathie augmente avec : (1) la durée du diabète — environ 50 % des type 2 et 80 % des type 1 ont une rétinopathie après 20 ans d'évolution ; (2) le déséquilibre glycémique chronique (HbA1c élevée) ; (3) l'HTA associée ; (4) la dyslipidémie ; (5) le tabac ; (6) la néphropathie diabétique (les deux microangiopathies évoluent en parallèle) ; (7) la grossesse. Bonne nouvelle : chaque % d'HbA1c en moins réduit le risque de complications microvasculaires de 21 % (étude UKPDS), même tardivement. Le diabète n'est jamais une « fatalité oculaire » — la prévention et le dépistage annuel changent radicalement le pronostic.
À quelle fréquence faire mon fond d'œil ?
Selon la HAS9 : annuel chez tout diabétique de type 1 (à partir de 5 ans d'évolution ou de l'adolescence si début pédiatrique) et annuel dès le diagnostic chez tout diabétique de type 2. Semestriel si rétinopathie débutante (R1, R2) ou diabète mal équilibré. Trimestriel si rétinopathie sévère (R3) ou évolution rapide. Avant et pendant chaque grossesse (au 1ᵉʳ trimestre puis tous les 3 mois) en cas de diabète préexistant. La téléophtalmologie (rétinophotographies par orthoptiste en cabinet, lecture par ophtalmologiste à distance) est désormais validée HAS et remboursée — elle facilite le dépistage en zones désertifiées.
Les injections dans l'œil, ça fait peur — comment ça se passe ?
L'injection intravitréenne est réalisée en cabinet d'ophtalmologie sous anesthésie locale par collyre, en quelques minutes. Le patient est allongé ou en position semi-assise, l'œil maintenu ouvert par un blépharostat. Une désinfection rigoureuse à la povidone iodée précède l'injection. Une aiguille très fine (30G) traverse la sclère à 3,5-4 mm du limbe et délivre 50 µL de solution anti-VEGF. La douleur est minime à modérée — un pincement bref. L'œil peut être flou pendant quelques heures, parfois rouge à l'endroit de l'injection. Effets indésirables sérieux rares : endophtalmie infectieuse (1/2000 à 1/5000 — d'où la désinfection stricte), déchirure rétinienne, hausse de pression intraoculaire transitoire. Vous devrez consulter en urgence en cas de douleur intense, rougeur, baisse de vision majeure, photophobie dans les 7 jours qui suivent.
Combien de temps faut-il maintenir les injections d'anti-VEGF ?
Au début du traitement de l'OMD, le protocole standard est 4 à 6 injections mensuelles d'attaque, puis espacement progressif selon la réponse anatomique (OCT maculaire) et fonctionnelle (acuité visuelle) — protocole PRN (Pro Re Nata, à la demande) ou Treat-and-Extend (intervalle progressivement allongé tant que la rétine reste sèche). En pratique, une partie des patients devient indemne au bout d'1 à 2 ans, une autre nécessite des injections d'entretien régulières (tous les 2 à 4 mois) pendant des années. Les molécules récentes (faricimab Vabysmo®, aflibercept haute dose Eylea HD®) permettent un espacement jusqu'à 16 semaines. La règle d'or : poursuivre le traitement tant que l'œdème ou la néovascularisation existent — arrêter trop tôt expose à une rechute.
Le laser pan-rétinien va-t-il abîmer ma vision ?
La photocoagulation pan-rétinienne (PPR) applique 1500 à 3000 impacts laser sur la rétine périphérique en épargnant la macula. Elle n'altère pas la vision centrale. Les effets secondaires concernent surtout : (1) une légère réduction du champ visuel périphérique ; (2) une baisse de la vision nocturne et de l'adaptation à l'obscurité — gênante pour la conduite nocturne intensive ; (3) une baisse de la sensibilité aux contrastes. Ces effets sont permanents mais compatibles avec une vie quasi normale. Le bénéfice — prévenir la cécité par hémorragie ou décollement de rétine — est très largement supérieur aux inconvénients. La PPR est indispensable en rétinopathie proliférante ; refuser le laser, c'est s'exposer à la cécité dans les mois ou années qui suivent.
Le diabète peut-il rendre aveugle ?
Oui, malheureusement, dans les formes graves non dépistées ou non traitées. La cécité diabétique survient par hémorragie intravitréenne massive, décollement de rétine tractionnel, glaucome néovasculaire, ou œdème maculaire chronique avec destruction des photorécepteurs maculaires. C'est la première cause de cécité acquise chez l'adulte avant 65 ans en France. Mais la quasi-totalité des cécités diabétiques sont évitables par le couple contrôle glycémique strict + dépistage annuel + traitement précoce. Depuis l'avènement des anti-VEGF (années 2000), les taux de cécité ont diminué significativement dans les pays développés. La cécité diabétique aujourd'hui est presque toujours le signe d'un défaut de suivi — accès aux soins limité, refus de traitement, déni de la maladie.
Je vois des « mouches volantes » depuis hier — c'est urgent ?
Chez un diabétique, l'apparition brutale et abondante de corps flottants (myodésopsies — petites taches noires ou « toiles d'araignées » qui flottent dans le champ visuel), surtout si accompagnée d'éclairs lumineux (phosphènes) ou d'une baisse de la vision, doit faire consulter en urgence (dans la journée, sinon le lendemain matin) un ophtalmologiste ou les urgences ophtalmologiques (CHU, certaines cliniques privées). Il peut s'agir d'une hémorragie intravitréenne (rupture d'un néovaisseau), d'un décollement de rétine, ou d'une déchirure rétinienne. Un seul corps flottant isolé, ancien, stable, dans un œil bien suivi par ailleurs, n'est pas une urgence — mais en parler à son ophtalmologiste lors du prochain dépistage.
Aller plus loin
- Diabète de type 2 — pilier1 — Pilier diabète : diagnostic, traitement, prévention. La rétinopathie est l'une des complications microvasculaires majeures à dépister.
- Complications du diabète de type 22 — Vue d'ensemble des complications micro- et macrovasculaires. La rétinopathie est la première cause de cécité acquise avant 65 ans.
- Alimentation et diabète de type 24 — Stratégie nutritionnelle pour maintenir HbA1c < 7 % et ralentir les complications microvasculaires.
- Activité physique et diabète10 — Pilier non médicamenteux de l'équilibre glycémique — réduit l'HbA1c de 0,5 à 0,8 %.
- Diabète gestationnel8 — Suivi ophtalmologique trimestriel pendant la grossesse chez la diabétique préexistante — la grossesse peut aggraver rapidement une rétinopathie.
- Dépistage du diabète : à quelle fréquence ?11 — Le diabète de type 2 est méconnu chez 1/4 des patients — au moment du diagnostic, jusqu'à 30 % ont déjà une rétinopathie débutante.
Sources et références
- HAS — Stratégie de prise en charge en cas de rétinopathie diabétique (juillet 2010, mise à jour 2023)12
Recommandation française de référence — classification ALFEDIAM des stades R0-R3, algorithme thérapeutique (contrôle métabolique, laser, anti-VEGF, corticostéroïdes), modalités de dépistage et de suivi. - HAS — Dépistage de la rétinopathie diabétique par lecture différée de photographies du fond d'œil (téléophtalmologie, 2014 maj 2022)9
Avis HAS sur la téléophtalmologie — rétinophotographies non mydriatiques par orthoptiste en cabinet ou centre de santé, lecture différée par ophtalmologiste, validation pour l'extension du dépistage en zones désertifiées. - ANSM — Lucentis® (ranibizumab), Eylea® (aflibercept), Vabysmo® (faricimab), Ozurdex® (dexaméthasone) : monographies13
Notices officielles françaises des principales molécules intravitréennes — indications dans la rétinopathie diabétique et l'œdème maculaire diabétique, schémas posologiques, contre-indications, effets indésirables. - INSERM — Diabète de type 2 et complications microvasculaires14
Dossier INSERM — physiopathologie du diabète de type 2 et de ses complications microvasculaires (rétinopathie, néphropathie, neuropathie), bases biologiques de la microangiopathie, perspectives de recherche. - Société Française d'Ophtalmologie (SFO) — Rapport « Rétinopathie diabétique » (2023)15
Société savante française de référence — recommandations actualisées sur la rétinopathie diabétique, classification, traitements (laser, anti-VEGF, corticostéroïdes, chirurgie), suivi. - Société francophone du diabète (SFD) — Référentiel sur les complications microvasculaires16
Société savante diabétologique francophone — recommandations sur la prise en charge globale du diabète, dépistage et prévention des complications oculaires, cibles glycémiques individualisées. - UKPDS Group — Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes (UKPDS 38, BMJ 1998)17
Étude UKPDS — démonstration que la baisse de la pression artérielle réduit significativement le risque de rétinopathie diabétique chez les patients DT2 hypertendus, complément du contrôle glycémique. - OMS — Diabetic eye disease (priority eye condition)18
Document OMS — la rétinopathie diabétique est l'une des causes prioritaires de déficience visuelle dans le monde ; recommandations sur le dépistage et la prise en charge dans les systèmes de santé. - DRCR.net (Diabetic Retinopathy Clinical Research Network) — Protocoles cliniques (Protocol T, Protocol I, Protocol V)19
Réseau international de recherche clinique — essais randomisés de référence comparant les anti-VEGF entre eux et au laser dans l'OMD, base scientifique des recommandations actuelles.
Réponses aux questions les plus courantes
<p>Le risque de rétinopathie augmente avec : (1) la <strong>durée du diabète</strong> — environ 50 % des type 2 et 80 % des type 1 ont une rétinopathie après 20 ans d'évolution ; (2) le <strong>déséquilibre glycémique</strong> chronique (HbA1c élevée) ; (3) l'<strong>HTA</strong> associée ; (4) la <strong>dyslipidémie</strong> ; (5) le <strong>tabac</strong> ; (6) la <strong>néphropathie diabétique</strong> (les deux microangiopathies évoluent en parallèle) ; (7) la <strong>grossesse</strong>. Bonne nouvelle : <strong>chaque % d'HbA1c en moins</strong> réduit le risque de complications microvasculaires de 21 % (étude UKPDS), <strong>même tardivement</strong>. Le diabète n'est jamais une « fatalité oculaire » — la prévention et le dépistage annuel changent radicalement le pronostic.</p>
Articles Connexes
Découvrez d'autres articles sur ce sujet

Antalgiques et lombalgie : paracétamol, AINS, opioïdes — ce qui marche vraiment
Lombalgie aiguë : paracétamol seul ≈ placebo (Cochrane 2023, PACE Lancet 2014), AINS courte durée en 1ʳᵉ intention HAS, myorelaxants optionnels, tramadol/codéine en 2ᵉ intention courte durée, opioïdes forts proscrits dans la lombalgie chronique non cancéreuse. Approche non médicamenteuse (kiné, exercice, TCC) au cœur de la stratégie. Sources HAS, ANSM, Cochrane, OFMA.
Neuropathie diabétique : symptômes, score DN4, prégabaline et duloxétine
Neuropathie diabétique : 30-50 % des diabétiques chroniques, polyneuropathie distale sensitivomotrice + neuropathie autonome. Dépistage clinique annuel par monofilament 10 g, diapason, score DN4. Traitements HAS 2020 — prégabaline, duloxétine, amitriptyline, gabapentine. Prévention du pied diabétique. Sources HAS, SFD, ANSM.

Lumbago aigu (coup de reins) : ce qu'il faut faire les 7 premiers jours
Lumbago aigu : douleur lombaire brutale, 84 % des adultes au moins une fois dans la vie. Guérison spontanée chez 90 % en 4-6 semaines selon la HAS 2019. Conduite : reprise rapide du mouvement (l'alitement est délétère), AINS courte durée si pas de contre-indication, pas d'imagerie de 1ʳᵉ intention, kinésithérapie active si douleur persiste à 4 semaines. Red flags : déficit moteur, troubles sphinctériens, fièvre, traumatisme.
Sourcé auprès d'autorités indépendantes
Cet article a été rédigé par Bilal YIKILMAZ, rédacteur en chef de cestlasante.com. Il n'est pas médecin : chaque recommandation ci-dessus s'appuie sur des sources médicales indépendantes, explicitement citées.
Autorités citées : HAS, INSERM, OMS.
Dernière révision éditoriale : .